Chapitre 6 : La liaison peptidique
Définition
Polypetides
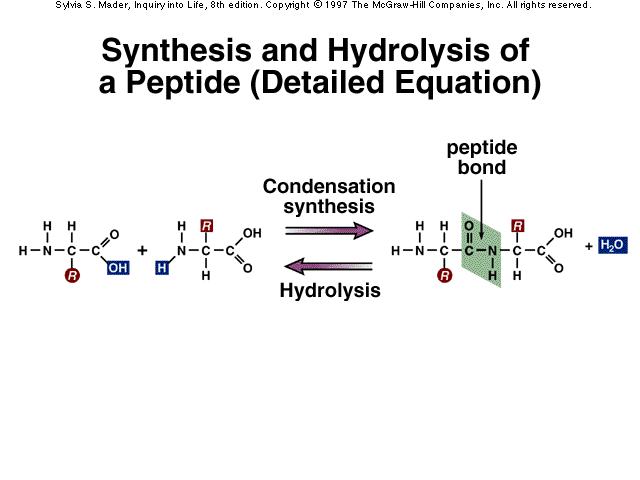
La synthèse du dipeptide Ala-Gly passe par la réaction entre le groupe –COOH d’une molécule de glycine et le groupe –NH2 d’une molécule d’alanine. Toutefois si les deux acides α-aminés sont introduits dans le milieu réactionnel, le dipeptide souhaité n’est pas le seul obtenu. En effet l’enchaînement entre les acides α-aminés peut être inversé, par la réaction entre le groupe –NH2 d’une molécule de glycine et le groupe –COOH d’une molécule d’alanine. Les molécules de glycines et celle d’alanine peuvent également réagir entre elles. Le tableau ci-dessous donne les dipeptides obtenus dans le mélange considéré :
Par ailleurs, le dipeptide possède également des groupes –COOH et –NH2 à ses extrémités et peut donc continuer à réagir pour conduire à la formation de tripeptide ou, en présence de suffisamment de quantité de matière, de polypetides. Sans précaution, un mélange de deux acides α-aminés aussi simples que l’alanine et la glycine peut ainsi conduire à une multitude de produits. Pour des raisons évidentes de purification et de rendement, cette situation est à éviter. Une stratégie de synthèse doit ainsi être mise en place pour obtenir uniquement le produit voulu.
Synthèse de Polypetides
Les protéines sont des exemple de polypeptides.
Hydrolyse