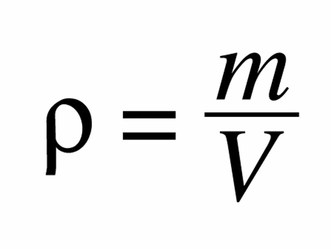Chapitre 4 : Le lait et ses constituants

Parmi les molécules présentes dans le lait, on peut distinguer :
_ les glucides de formules Cx(H20)y, aussi appelés hydrate de carbone.
Ex : le lactose C12(H20)11
_ les lipides qui sont des corps gras.
Ex : triglycerides
_ les protéines qui sont des molécules formées par liaisons entre différents acides aminés.
Ex : la caséine.
_ les vitamines qui sont indispensables au bon fonctionnement et à la croissance de l’organisme.
Certaines sont solubles dans l’eau (hydrosolubles), C et groupe B
D’autres sont solubles dans les lipides (liposolubles), A, D, E et K.
Ex : la vitamine D permet de fixer le calcium sur les os.
L'atome et les ions
Un atome est constitué par un noyau contenant des protons et des neutrons entourés d’un nuage contenant les électrons.
On utilise souvent la représentation symbolique du noyau

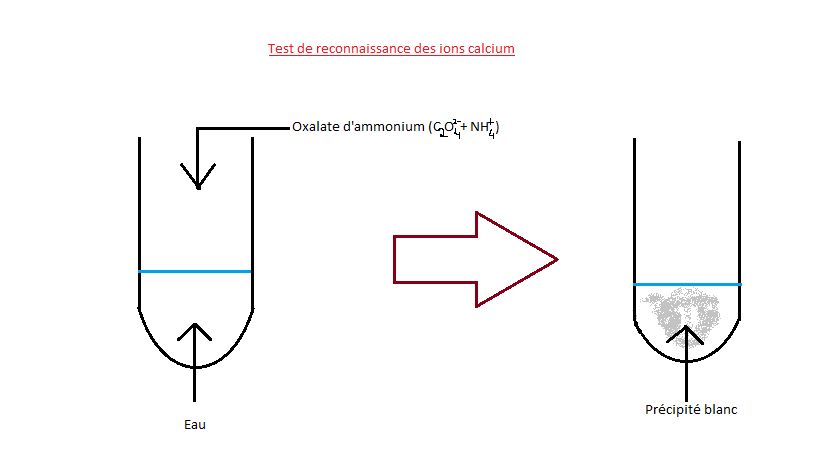
Un ion se forme lorsque qu’un atome gagne ou perd un ou plusieurs électrons. On distingue les cations (ions positifs) des anions (ions négatifs).
Les molécules
Les molécules résultent de l'association d'atomes.
Il existe différentes façons de représenter une même molécules.
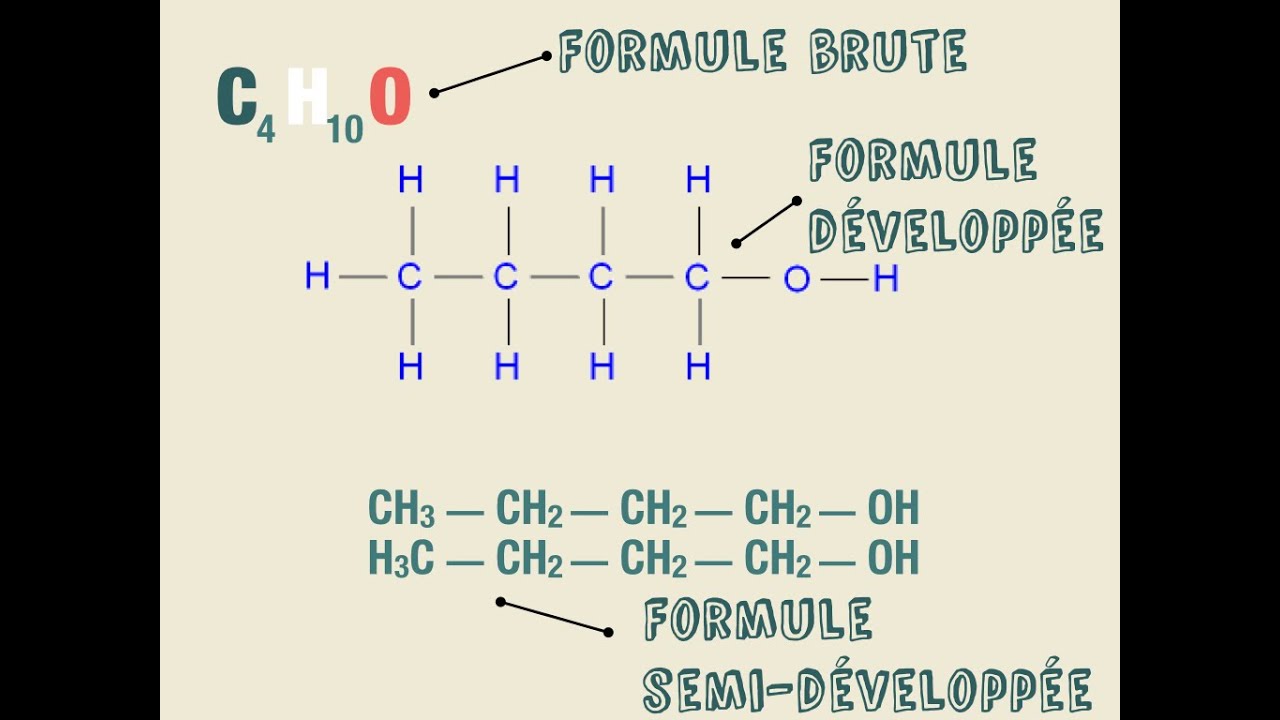
Remarque : Des molécules ayant même formule brute mais une formule développée différentes sont dites isomères.
Les solutions
Les étiquettes des bouteilles de lait indiquent généralement la composition de ceux-ci avec les masses des différents constituants pour 100mL de liquide.
On peut en déduire la concentration massique Cm

Rappel : on a plus souvent recourt à la mole en chimie.
La mole représente la quantité de matière, cela nous renseigne sur le nombre réelle de molécules que contient un échantillon.
on peut la calculer avec

Calcul d'une masse molaire moléculaire => somme des masses molaires atomiques.
Exemple : M(H2O) = 2xM(H) + M(O) = 2x1+16 = 18 g/mol.
On peut également calculer la concentration molaire C (en mol/L)

Remarque : 1L d’eau pèse 1 kg, quelle est la masse d’un litre de lait ?
En moyenne 1030 g/L, cela représente sa masse volumique.